液体および気体中の電流
液体中の電流
 金属導体では 電気 自由電子の指向性運動によって形成され、導体を構成する物質には変化が起こらない。
金属導体では 電気 自由電子の指向性運動によって形成され、導体を構成する物質には変化が起こらない。
電流の通過によって物質の化学変化が起こらないこのような導体は、第一級導体と呼ばれます。これらには、すべての金属、石炭、およびその他の多くの物質が含まれます。
しかし、自然界には、電流の通過中に化学現象が発生するような電流の導体も存在します。これらの導体は、第 2 種導体と呼ばれます。主に、酸、塩、塩基のさまざまな水溶液が含まれます。
ガラス容器に水を注ぎ、そこに硫酸(または他の酸やアルカリ)を数滴加え、次に 2 枚の金属板を用意してワイヤーを取り付け、これらの板を容器の中に下げ、電流を接続するとします。スイッチと電流計を介してワイヤーのもう一方の端に供給すると、溶液からガスが放出され、回路が閉じている限りガスが放出され続けます。酸性化した水は確かに導体です。さらに、プレートは気泡で覆われ始めます。すると、これらの泡がプレートから剥がれて出てきます。
溶液に電流を流すと化学変化が起こり、ガスが発生します。
これらは第 2 タイプの電解質の導体と呼ばれ、電流が電解質を通過するときに電解質内で起こる現象が電気分解です。
電解液に浸した金属板は電極と呼ばれます。電流源の正極に接続されている一方はアノードと呼ばれ、負極に接続されているもう一方はカソードと呼ばれます。
液体導体中の電流の通過を決定するものは何ですか?このような溶液(電解質)では、溶媒(この場合は水)の作用下で酸分子(アルカリ、塩)が2つの成分に分解され、分子の一方の部分は正の電荷を持ち、もう一方の部分は正の電荷を持っていることがわかります。マイナスのもの。
電荷を持った分子の粒子をイオンと呼びます。酸、塩、アルカリが水に溶けると、溶液中に正と負の両方のイオンが大量に発生します。
これで、なぜ電流が溶液を通過したのかが明らかになるはずです。電流源に接続された電極間には、 電位差言い換えれば、一方はプラスに帯電し、もう一方はマイナスに帯電していることが判明しました。この電位差の影響で、正イオンは負極、つまりカソードに向かって混合し始め、負イオンはアノードに向かって混合し始めます。
したがって、イオンの無秩序な動きは、一方向の負イオンと別の方向の正イオンの秩序だった逆の動きになりました。この電荷移動プロセスは電解質を通る電流の流れであり、電極間に電位差がある限り発生します。電位差がなくなると、電解質を流れる電流が止まり、イオンの規則正しい動きが妨げられ、再び無秩序な動きが始まります。
例として、硫酸銅 CuSO4 の溶液中に銅の電極を下げた状態で電流が流れるときの電気分解の現象を考えてみましょう。
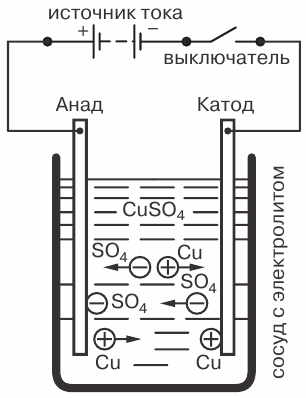
硫酸銅の溶液に電流が流れるときの電気分解現象: C - 電解液の入った容器、B - 電流源、C - スイッチ
電極へのイオンの逆移動も起こります。正イオンは銅イオン (Cu)、負イオンは酸残留物 (SO4) になります。銅イオンは、陰極に接触すると放出されます(失われた電子が結合します)。つまり、銅イオンは中性の純銅分子に変換され、最も薄い(分子状)状態で陰極に堆積します。 )層。
アノードに到達したマイナスイオンも排出されます(過剰な電子を供与します)。しかし同時に、それらはアノードの銅と化学反応を起こし、その結果、銅の分子Ctiが酸残基SO4に付加され、硫酸銅の分子CnasO4が形成され、アノードに戻されます。電解質。
この化学プロセスには長い時間がかかるため、銅が陰極に堆積し、電解液から放出されます。この場合、電解質は、カソードに移動した銅分子の代わりに、第 2 の電極であるアノードの溶解により新しい銅分子を受け取ります。
銅の代わりに亜鉛電極を使用し、電解液が硫酸亜鉛 ZnSO4 の溶液である場合にも、同じプロセスが行われます。亜鉛もアノードからカソードに移動します。
したがって、金属と液体導体中の電流の違いは、金属では電荷キャリアが自由電子のみであるという事実にあります。電解質中にあるときはマイナス電荷 電気 逆に帯電した物質の粒子、つまり反対方向に移動するイオンによって運ばれます。電解質がイオン伝導性を持つと言われるのはこのためです。

電気分解の現象は、化学電流源を研究し改善するために数多くの実験を行った B. S. ヤコビによって 1837 年に発見されました。ヤコビは、硫酸銅の溶液中に置かれた電極の 1 つが、電流が流れると銅でコーティングされることを発見しました。
この現象は電鋳と呼ばれ、現在では非常に大きな実用化がなされています。この一例は、ニッケルめっき、金めっき、銀などの他の金属の薄層で金属物体をコーティングすることです。
気体中の電流
気体(空気を含む)は、通常の状態では電気を通しません。たとえば、目標 架空線用電線互いに平行に吊り下げられているため、空気層によって互いに隔離されています。
しかし、高温、大きな電位差、その他の理由の影響下で、液体導体と同様に気体はイオン化します。つまり、気体分子の粒子がその中に大量に現れ、電気のキャリアとして通過に寄与します。ガスを流れる電流。
しかし同時に、気体のイオン化は液体導体のイオン化とは異なります。液体中で分子が 2 つの帯電部分に分裂すると、気体中ではイオン化の作用により電子が常に各分子から分離され、イオンは分子の正に帯電した部分の形で残ります。
気体は導電性を失うため、気体のイオン化を停止するだけで済みますが、液体は常に電流の導体のままです。したがって、ガスの導電率は外部要因の作用に依存する一時的な現象です。

ただし、別のことがあります 放電の種類アーク放電または単に電気アークと呼ばれます。電気アーク現象は、19 世紀初頭にロシア初の電気技師 V. V. ペトロフによって発見されました。
V.V. 数多くの実験を行った結果、ペトロフは、電流源に接続された2つの石炭の間で、明るい光を伴う連続的な放電が空中に現れることを発見しました。 V.V.ペトロフは著書の中で、この場合「暗い静けさも十分に明るく照らすことができる」と書いています。こうして、初めて電灯が得られ、これは別のロシアの電気技師、パーベル・ニコラエヴィチ・ヤブロチコフによって実用化された。
「スヴェシュト・ヤブロチコフ」の作品は、電気アークの使用に基づいており、当時の電気工学に真の革命をもたらしました。

アーク放電は現在、スポットライトや投影装置などの光源として使用されています。アーク放電の温度が高いため、次のような用途に使用できます。 アーク炉装置... 現在、非常に高い電流で駆動されるアーク炉は、鋼、鋳鉄、合金鉄、青銅などの溶解に多くの産業で使用されています。そして 1882 年に、NN ベナルドスが金属の切断と溶接に初めてアーク放電を使用しました。
ガスパイプ、蛍光灯、電圧安定器では、電子ビームとイオンビームを得るために、いわゆるグローガス放電が行われます。
スパーク放電 表面が研磨された 2 つの金属ボールからなる電極を備えた球状のスパーク ギャップを使用して、大きな電位差を測定するために使用されます。ボールは離れて移動し、測定可能な電位差がボールに適用されます。次に、ボール間で火花が通過するまで、ボールを近づけます。ボールの直径、ボール間の距離、空気の圧力、温度、湿度がわかっているので、特別な表に従ってボール間の電位差を見つけます。この方法では、数万ボルトオーダーの電位差を数%の精度で測定することが可能です。
