電気毛細管現象
電解質の表面が帯電している場合、その表面の表面張力は隣接する相の化学組成だけでなく、それらの電気的特性にも依存します。これらの特性は、表面電荷密度と界面での電位差です。
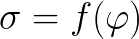
この現象の表面張力の電位差への依存性 (e) は、電気毛管曲線で表されます。そして、この依存性が観察されるまさに表面的な現象は、電気毛細管現象と呼ばれます。
電極と電解質の界面で電極電位を何らかの方法で変化させます。この場合、ここには外部起電力はまったくありませんが、金属表面には表面電荷を形成し、電気二重層の存在を引き起こすイオンが存在します。
同じように荷電したイオンは界面の表面全体で互いに反発し、液体分子の収縮力を補償します。その結果、表面張力は、電極に過剰な電位が存在しない場合よりも低くなります。
逆符号の電荷が電極に印加されると、イオンの相互反発力が減少するため、表面張力が増加します。
反発イオンの静電力によって引力が絶対的に補償される場合、表面張力は最大に達します。電荷を供給し続けると、新しい表面電荷が発生して成長するため、表面張力は減少します。
場合によっては、電気毛細管現象の重要性が非常に大きくなります。これらにより、液体と固体の表面張力を変化させたり、付着、湿潤、分散などのコロイド化学プロセスに影響を与えることが可能になります。
この依存性の定性的な側面にもう一度目を向けてみましょう。熱力学的には、表面張力は単位表面を形成する等温プロセスの仕事として定義されます。
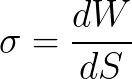
表面に同じ名前の電荷がある場合、それらは静電気で互いに反発します。静電反発力は表面の接線方向に向けられ、とにかくその面積を増やそうとします。その結果、帯電した表面を伸ばす仕事は、同様ではあるが電気的に中性の表面を伸ばすのに必要な仕事よりも少なくなります。
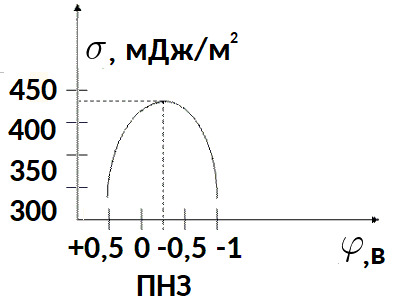
例として、室温での電解質水溶液中の水銀の電気毛細管曲線を考えてみましょう。
表面張力が最大になる時点では、電荷はゼロになります。これらの条件下では、水銀表面は電気的に中性です。したがって、電極の表面張力が最大となる電位がゼロ充電電位 (ZCP) です。
ゼロ電荷の電位の大きさは、液体電解質の性質と溶液の化学組成に関係します。表面電位がゼロ電荷の電位よりも低い電気毛管曲線の左側は、陽極分岐と呼ばれます。右側がカソード分岐です。
電位の非常に小さな変化(0.1 V程度)により、表面張力に顕著な変化(1平方メートルあたり10 mJ程度)が生じる可能性があることに注意してください。
表面張力の電位依存性はリップマン方程式で説明されます。
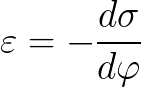
電気毛細管現象は、金属へのさまざまなコーティングの塗布に実際に応用されており、液体による固体金属の濡れを制御することが可能になります。リップマン方程式により、電気二重層の表面電荷と静電容量を計算できます。
界面活性剤のイオンには特異的な吸着力があるため、電気毛管現象を利用して界面活性剤の表面活性が測定されます。溶融金属(亜鉛、アルミニウム、カドミウム、ガリウム)中では、その吸着能力が決まります。
電気毛細管理論は、ポーラログラフィーにおける最大値を説明します。電極の濡れ性、硬度、摩擦係数の電位への依存性も、電気毛細管現象を指します。

